基礎研究
-
肝細胞癌のFFPE標本を対象とした網羅的プロテオーム解析
肝細胞癌は日本国内で毎年3万人以上の方が診断される病気で、ウイルス性肝炎や脂肪性肝炎などの肝疾患が発生の原因となることが知られております。しかし、どのように癌が発生するのかという具体的な発癌メカニズムは未だ十分に理解されておりません。また、肝細胞癌の治療においては、薬物療法の効果が他の癌に比べて小さいことや再発率が高いことが問題となっております。
手術で切除した癌やその周囲の肝臓組織は、ホルマリン固定パラフィン包埋(formalin-fixed paraffin-embedded:FFPE)標本という形で保管されます。体の外に取り出された癌や肝臓組織は、何もしないと時間経過とともに変性してしまいますが、ホルマリンという薬剤に漬けることによって、その変化を防ぐことができ、ロウのような素材であるパラフィンの中に埋め込むことで長期保存が可能になります。通常診療では、このFFPE標本は病理医による病理診断に利用されます。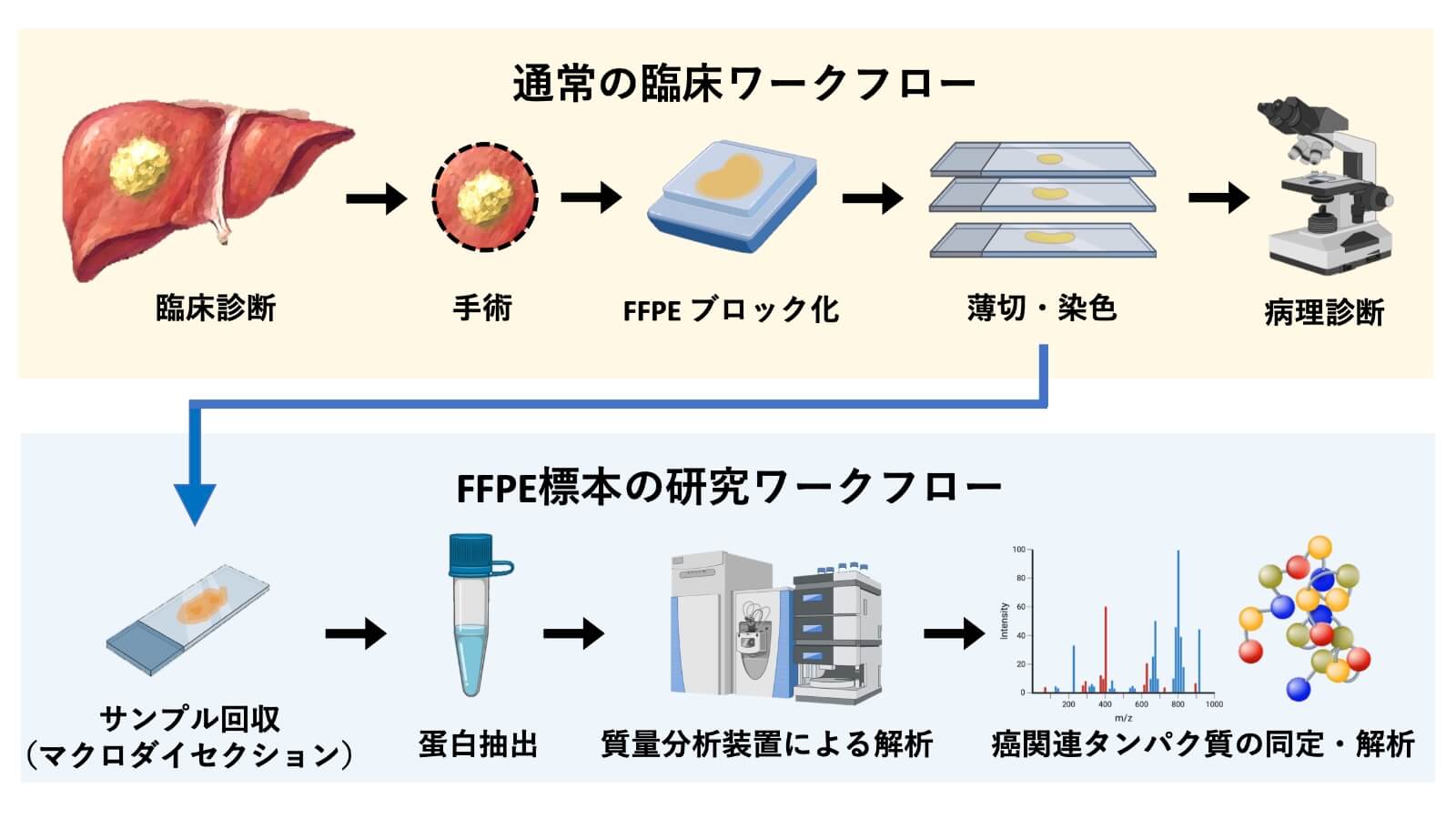
近年、このFFPE標本から癌に関連するタンパク質を調べる方法が開発され、注目を集めています。長い間、FFPE標本はホルマリンによって固定されてしまっているため、タンパク質を調べることは難しいとされてきました。しかし、タンパク質の抽出方法が改良され、質量分析装置という解析機器の質が著しく向上したことで、これまで検出することができなかった癌に関わる微量なタンパク質を見つけることができるようになりました。また、癌の発生メカニズムには遺伝子の変異が強く関わっていることが知られています。そのため、腫瘍細胞やその他の正常細胞の遺伝子情報を調べることは、癌研究を行う上で非常に重要です。遺伝子解析においても、次世代シークエンサーという技術が開発され短時間で多くの遺伝子を調べることが可能になりました。
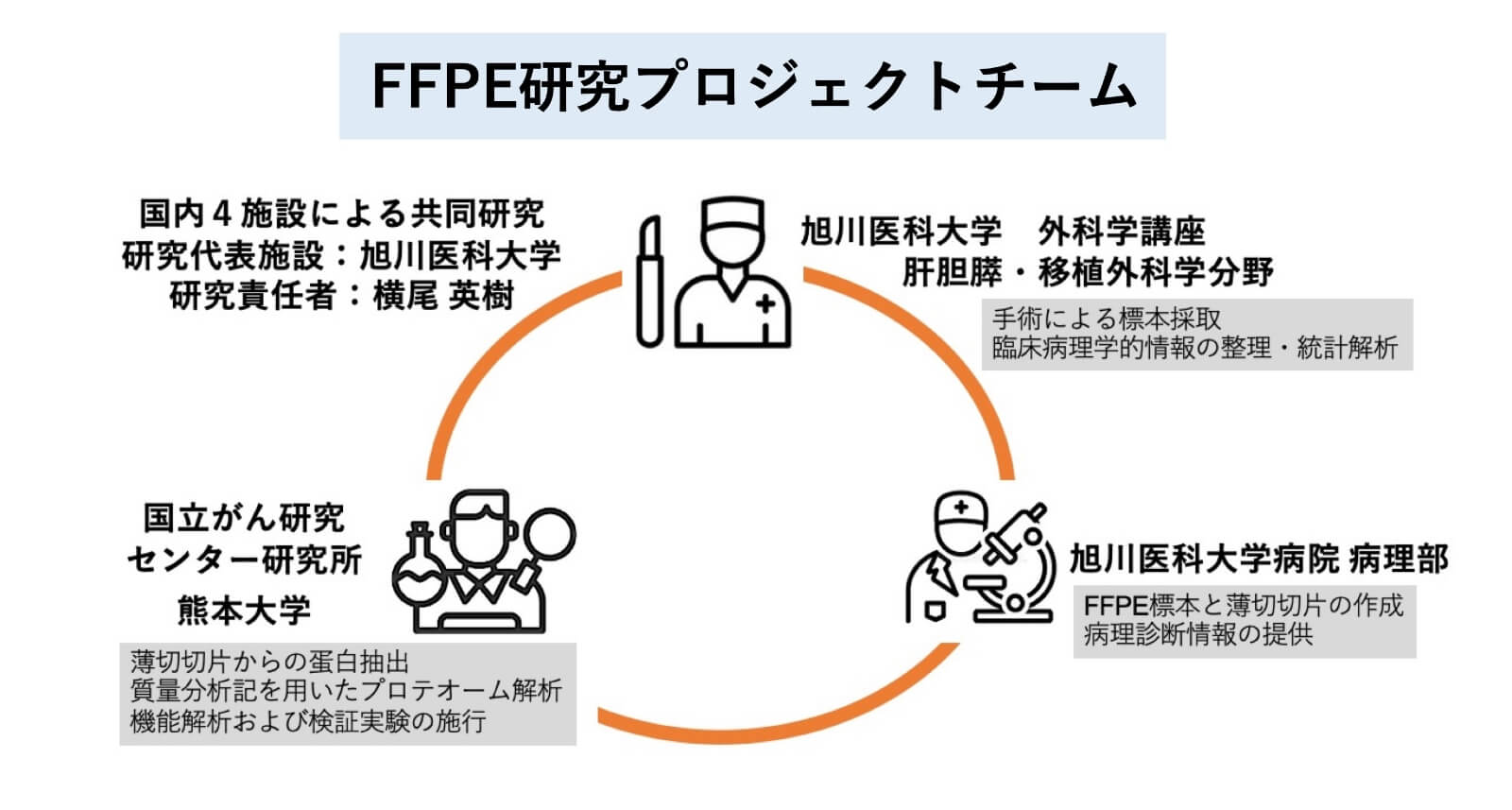
旭川医科大学肝胆膵・移植外科は、これらの新しい研究対象や解析技術を利用し、国内の共同研究機関と連携しながら、癌に関連するタンパク質や遺伝子の解析を行っております。我々は、この研究を推し進めることで、肝細胞癌の発生原因や再発のメカニズム、抗がん剤の効果が患者さん毎に異なる理由、といった臨床的な課題や疑問を解決し、新たな治療法の開発や個別化した医療の実現を目指しています。
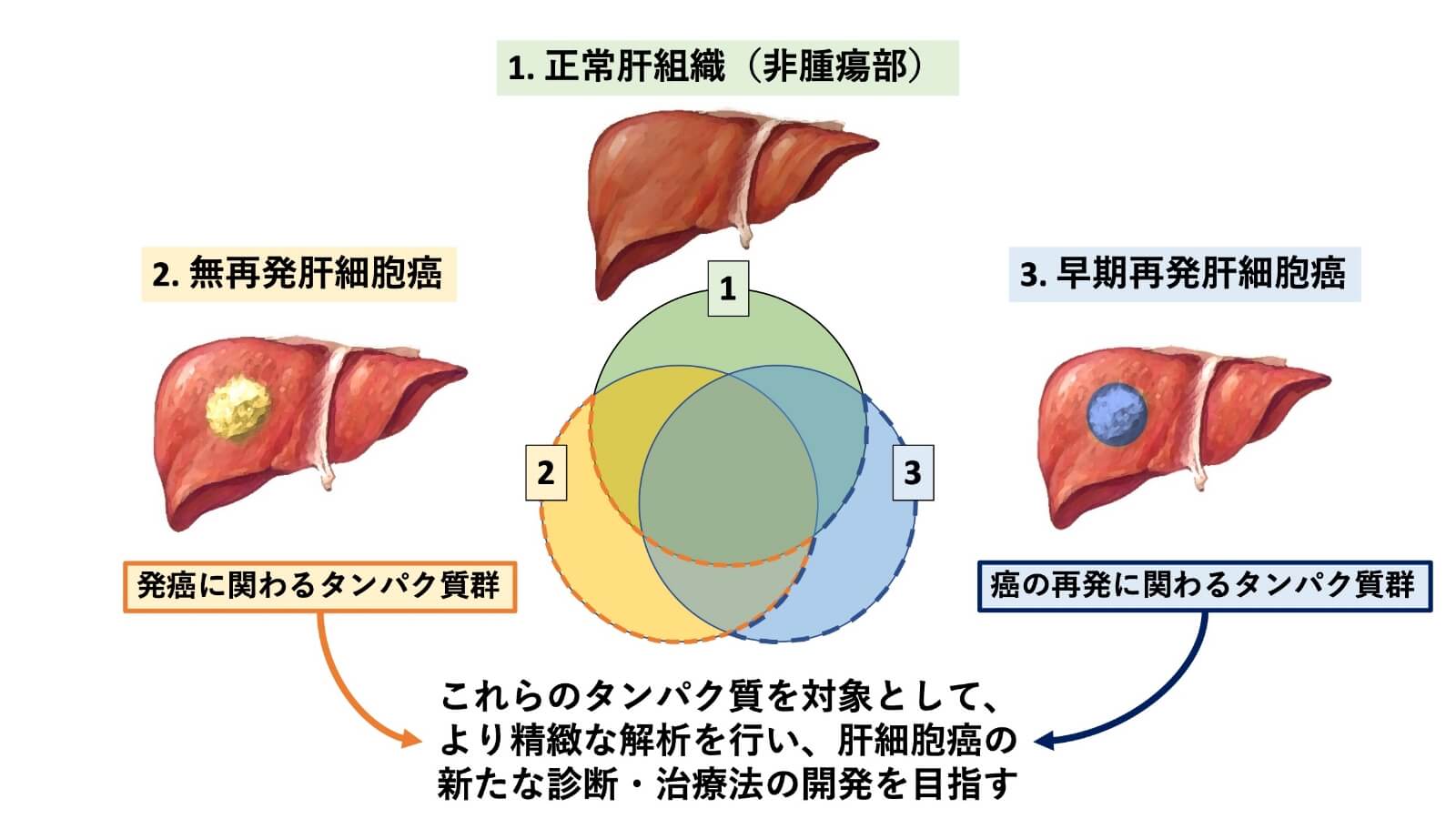
-
肝細胞癌に対するFABP5を標的にした新規治療法の開発
近年、肝細胞癌に対する治療成績は分子標的薬の開発や手術技術の進歩により向上しつつあります。しかし、薬物療法の効果は未だ十分ではなく、新たな治療薬剤の開発が求められています。
横尾英樹教授らのこれまでの研究により、肝細胞癌の細胞には表皮型脂肪酸結合蛋白(FABP5)というタンパク質が多く存在し、がんの悪性化に関与していることが明らかとなりました。この知見を踏まえ、旭川医科大学肝胆膵・移植外科はFABP5を起点とした新たな治療薬の開発を目指し、研究を行っております。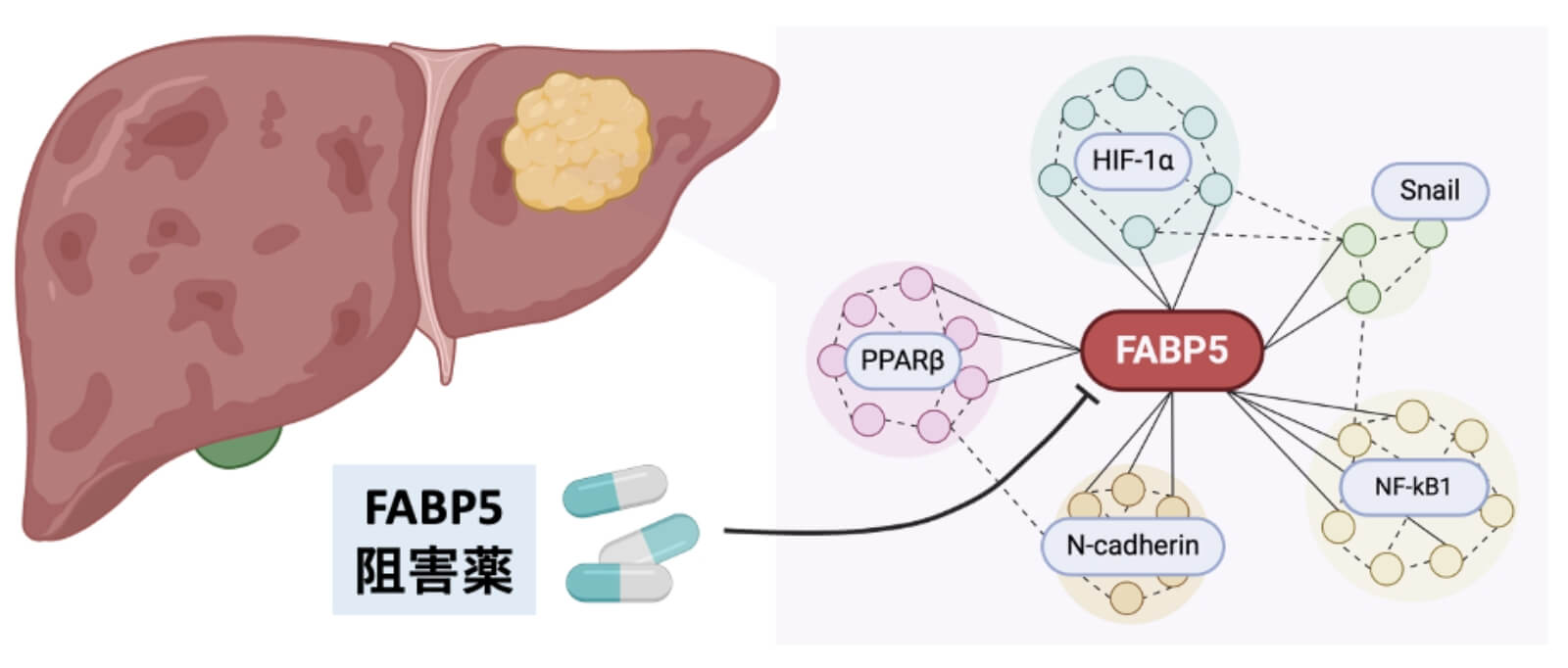
本研究の一環として行われた、がんの細胞株を対象とした実験によって、FABP5の阻害薬ががん細胞の増殖を抑制することを示し、その薬理作用の一部を解明しました。この研究成果を各種学会で発表し、学会賞(日本患者由来がんモデル学会2022: ポスター賞)やAward(Human Proteome organization 2022 : Presentation Award)を受賞しています。
現在は、動物や臨床検体を移植したがんモデルマウスを対象として、より実臨床に近い条件下での研究を進めており、肝細胞癌に対する総合的なFABP5阻害薬の有効性を検証中です。将来的な臨床応用を目標として、研究を継続しております。 -
胆管癌の進展度範囲診断におけるゲノム変異情報付加の有用性
胆管癌は完全切除が唯一の根治治療ですが、画像や生検による術前の正確な進展度範囲診断や術中の迅速診断による切除断端陰性の判定は必ずしも容易ではありません。胆管内には原発巣から連続して、あるいはスキップして派生した病変の他に、多発病変、さらに胆管閉塞やドレナージによって二次的に生ずる再生異型が存在するため、熟練した病理医をもってしても客観性のある評価が難しいことがあります。旭川医科大学肝胆膵・移植外科は旭川医科大学消化器内科水上研究室と共同し、胆管癌の切除材料を用いて胆道上皮内病変の形態的特徴と長軸方向への分布・遺伝子変異を詳細に解析し、より正確な胆管癌の進展度範囲診断法の開発を目指し、研究を行っております。
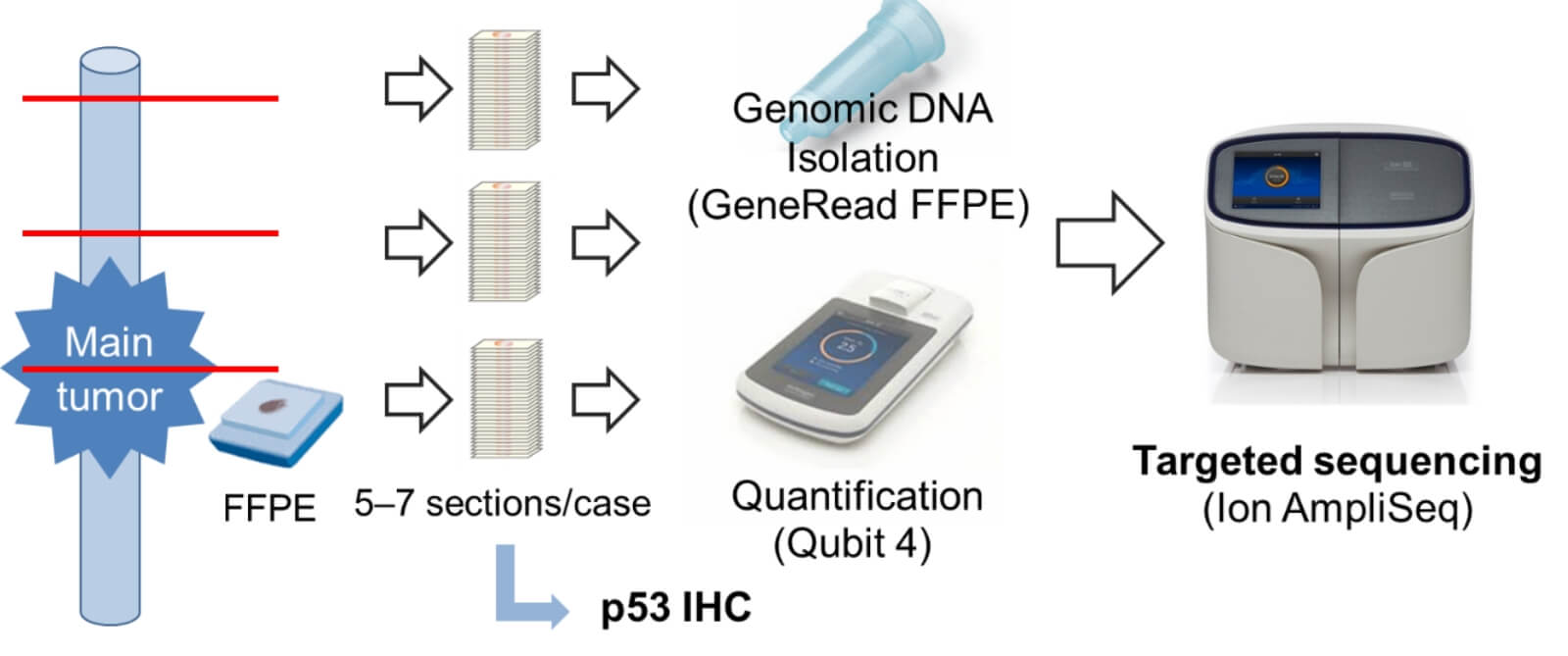
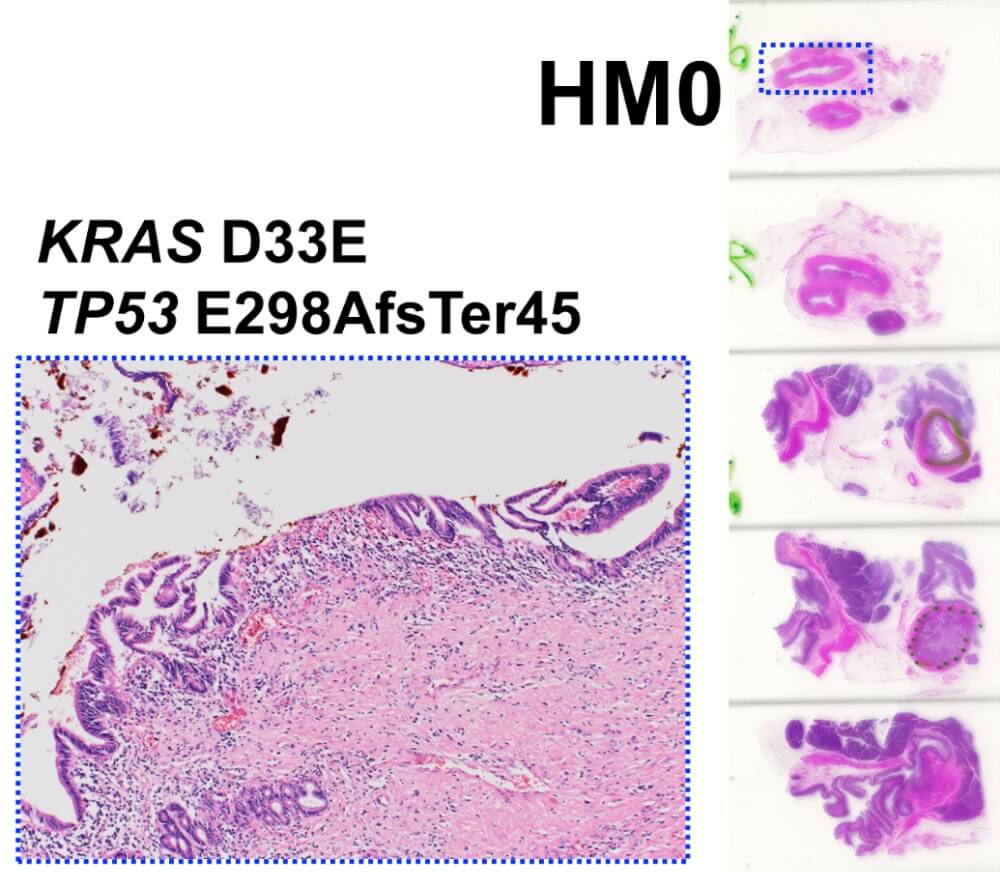
ターゲットシーケンスは日本人の胆管癌に関する既報を参考に、高頻度な変異がみられた20遺伝子を搭載したカスタムパネルを用いて、各部位におけるドライバー変異情報を取得しています。現在までの成果としては、胆管がんはTP53変異を持つことが多く、ターゲットシークエンスで検出することができること、病理学的に切除断端陰性と判定された症例においても、TP53等の変異が切除断端で検出されることがあり、根治切除後の再発に関わる可能性のあることが明らかとなりました。将来的な臨床応用を目標として、研究を継続しております。
-
大腸癌肝転移の集学的治療の発展
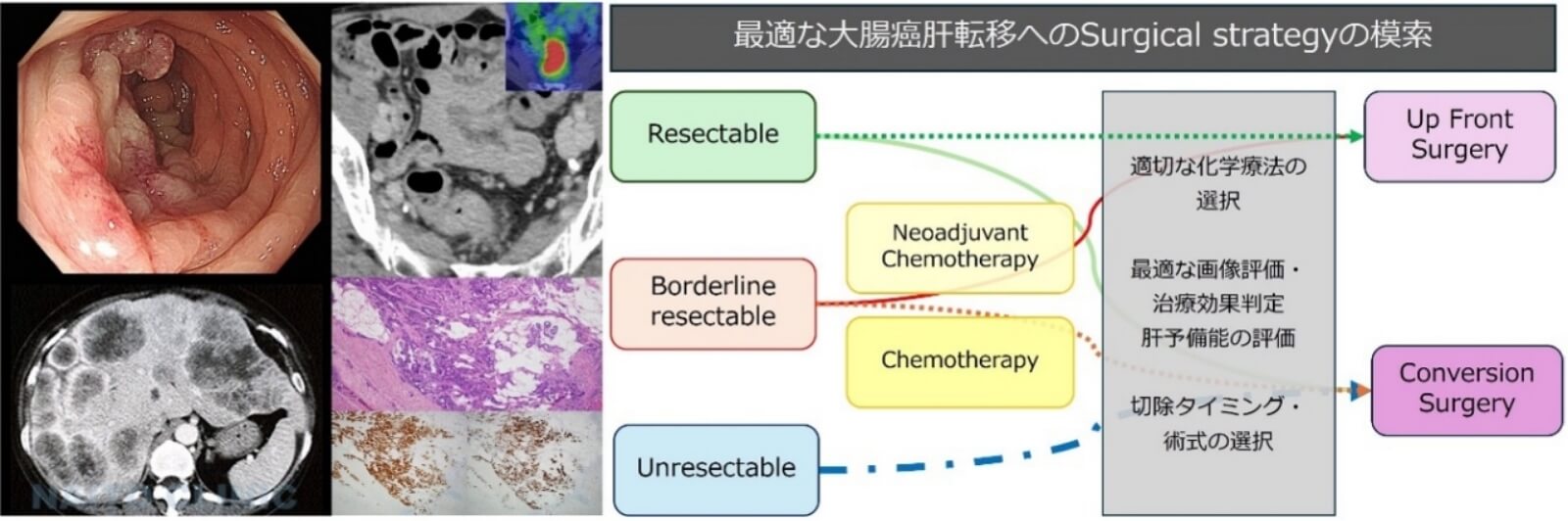
大腸癌肝転移の現状大腸癌は,本邦の全国癌登録統計データに基づくと,部位別罹患数1位,部位別死亡数2位と非常に頻度が高い癌腫です [1].中でも,大腸癌肝転移は大腸癌の遠隔転移部位として最多であり,大腸癌研究会・全国登録によると,診断時に10.9%で同時性肝転移が発覚し,すでに根治切除不能である症例は75-90 %と報告されています [2, 3].一方で,大腸癌肝転移に対する唯一の根治療法は肝切除であり,初回肝切除後の5年生存率は35-58 %と比較的良好です.最近では様々な化学療法を組み合わせた集学的治療の発展に伴い,肝転移症例の治癒切除率・予後は向上しており,切除不能肝転移症例に対する薬物療法後のConversion surgery症例でも,5年生存率が33-55 %と初回肝切除群と遜色のない成績が報告されています [4, 5].しかしながら,5年内の再発率は70-80 %と高率であり,治癒切除後の再発率は依然として高いのも現状です [6, 7].
進歩する大腸癌肝転移に対する適切な集学的治療の探求どのような症例に対して,どのような治療方法を,いつ選択するのか,症例に合わせて病態と患者背景を理解し,適切な治療法を選択することは個別化医療(personalized medicine)の観点で非常に重要です. 我々は,これまでに当科で得られた臨床病理学的データを活用し,様々な最新の知見と統合した解析を継続して施行しており,大腸癌肝転移に対する適切な治療方法についての臨床研究を行っています.
-
大腸癌肝転移の病理組織学的増殖パターンの病態解析
大腸癌肝転移巣はどのように浸潤・増殖するのか(Histopathological growth patternの研究・解析)病理組織学検査所見で得られた知見から,その病態や分子生物学的背景に迫ることは非常に重要ですが,これまで大腸癌肝転移の病理組織学検査指標として有用な項目の報告は本邦では少なく,現行の「治療ガイドライン」や「癌取り扱い規約」でも明記はされていません.
近年,大腸癌の病理組織学的な評価項目として,その浸潤増殖様式に着目したHistopathological growth pattern(HGP)が注目されています [8, 9].
大腸癌の癌細胞は門脈を経由して肝臓に到達し,肝類洞の内腔に接着します.その後,肝類洞内皮細胞(LSEC)の柵状突起から滲出しながら移動していきますが,その後肝内で大きく2種類の増殖パターン(Desmoplastic HGPとReplacement HGP)を取ることが明らかとなってきました [10].- Desmoplastic HGP:転移した腫瘍細胞が宿主肝との境界面でせめぎあい,肝門板を破壊することで宿主の免疫細胞が動員され,活性化線維芽細胞や沈着線維が細胞外マトリックスの再構築を誘導し,被膜を形成されます.
- Replacement HGP:高い遊走能と浸潤能を有する腫瘍細胞が宿主の正常肝細胞と相互に作用しながらLSECなどと共生することで,腫瘍に対する免疫微小環境を寛容状態にリモデリングし,既存の肝血管を利用して浸潤増殖します(肝構造の破壊・広範な免疫浸潤を引き起こさない)
HGPのパターンにより,再発・予後が異なることが明らかとなっており,当科の臨床病理学的解析でも、既報と同様に正常肝細胞にカモフラージュして浸潤増殖すると考えられるReplacement HGPは再発・予後不良因子になることが明らかとなってきました。
このHGPの浸潤・形成・増殖メカニズムを明らかにすることは,大腸癌肝転移治療に大きく寄与する可能性があります [8-10].HGPに関する今後の展望現在,当科では手術で切除した病理検体を利用し,HGPに基づいて,更なる病理組織学的分析や遺伝子次世代シーケンシング(Next-Generation Sequencing:NGS)を施行し,肝転移巣の病理組織学的・遺伝的背景の検索,ドライバー遺伝子の発見・解明を行っています. これらの研究解析結果を活かして,既存の薬物治療や外科切除・局所治療などの集学的治療方針へ新しい知見を提言することやHGPのメカニズム形成に作用する新規治療薬を開発することが,我々の研究の大きな一つの目標です.
Reference- https://ganjoho.jp/reg_stat/statistics/data/dl/index.html#a14
- https://www.jsccr.jp/registration/report.html [Accessed 2023 Aug 31]
- Ann Surg Oncol. 2005 Aug;12(8):637-45
- Ann Gastroenterol Surg. 2019 Jan 14;3(1):50-56.
- Ann Surg Oncol. 2014 Jun:21 Suppl 3:S405-13.
- Curr Opin Oncol 22:364-373, 2010
- J Hepatobiliary Pancreat Sci 19:72-84, 2012
- Br J Cancer. 2017 Nov 7; 117(10): 1427–1441.
- Br J Cancer. 2022 Oct 5; 127(6): 988–1013.
- World J Gastroenterol 2022 July 14; 28(26): 3101-3115
科研費- 患者由来がんモデルを用いた肝細胞癌に対するFABP5を標的にした新規治療法の開発 基盤研究C 横尾英樹 2020-2024 旭川医科大学倫理委員会承認番号:21178
- 膵管内乳頭粘液性腫瘍の進展を担う分子機構の解明 基盤研究C 今井浩二 2020-2023
- 胆道癌における形態別にみた上皮内病変の胆管内分布とclonality 若手研究 高橋裕之 2021-2024
- 全膵のゲノム異常監視による膵癌術後再発の予測 基盤研究C 今井浩二 2023-2025
